1918年3月,美国堪萨斯州莱利堡的军营(Camp Funston)中,超过100名士兵感染了类似流感的疾病,一周之内,病例增加5倍。如今,回溯一个世纪前的1918年大流行,这一军事基地通常是记录这场灾难性疫情的起点,尽管它的源头仍然是谜。
这场大流感也被称为“西班牙大流感”,原因仅在于西班牙首先报道了这场流感的真实情况。美国历史学家约翰·马克斯韦尔·汉密尔顿就曾谈到,“西班牙大流感”的称呼十分不妥。他认为,彼时正值第一次世界大战,只是因为西班牙当时是中立国,没有战时新闻审查制度。而交战国美国、德国、英国、法国等,都有那样的新闻审查制度,他们不想让大流感的消息影响战争。
1918年至1919年,三波疫情感染了当时全球近1/3(约5亿人)的人口。严重性超乎想象,相比其他大流行的致死率(小于0.1%),1918年大流感致死率高于2.5%。最终造成多少人死亡?持续的研究认为,这一流行病的全球死亡率估计持续向上修正。

20世纪20年代的计算结果为2150万左右。1991年的一篇论文将死亡人数修订为2470万至3930万之间。2000年之后,这一数字继续向上修正至大约有5000万。然而,必须承认,即使是如此巨大的数字也可能大大低于实际死亡人数,目前有观点认为有1亿以上的人口付出了生命的代价。
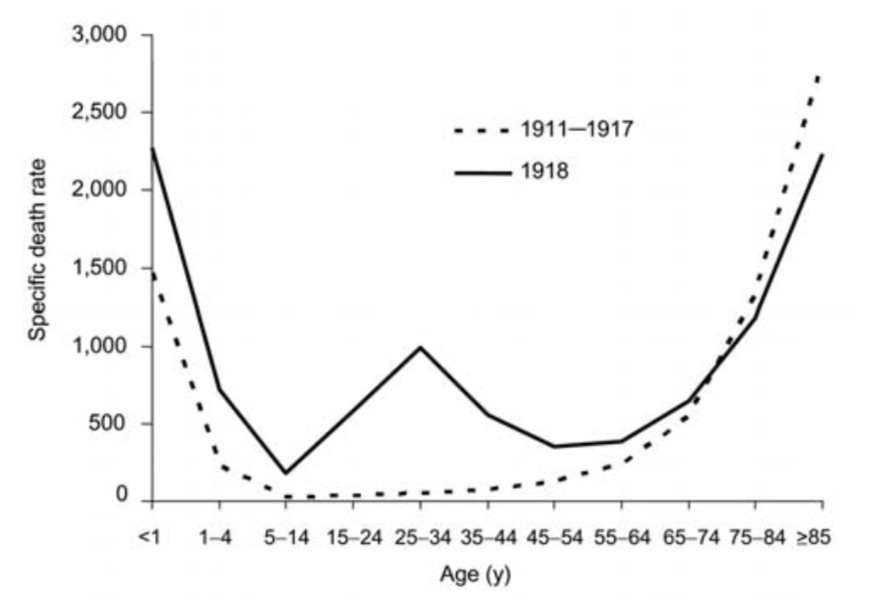
更令科学界至今不解的是,1918年大流行杀死了大量健康的年轻人。它的死亡曲线显示出了独特的、此前从未记录过的“W型”曲线,除了幼年和老年人群,20-40岁人群新增加了一个死亡高峰。实际上,近一半的1918年大流感死亡来自该年轻群体。
自然界和人类社会的第一次大冲突留下很多谜团。无论是对传染性病原体的认识,还是科学研究工具,几代科学家的努力和付出最终让所有这些产生了一个又一个突破。对1981年出生于法国西南部城市蒙托邦的SébastienCalvignac-Spencer来说,揭开谜团的交接棒已经到了他们这代人的手中。
“我对过去几个世纪呼吸道病原体的进化很感兴趣,1918年大流行病毒当然也在我们的‘雷达’范围内。”Spencer在接受澎湃新闻(www.thepaper.cn)记者采访时谈到,他们在一开始搜寻那些保存在病例博物馆的标本时,“相当于撒下了一张相当大的网,但我们一度认为可能找不到1918年大流感时期的样本。”
Spencer说最终结果是幸运的。研究团队在柏林Charité和维也纳Narrenturm的病理博物馆标本中找到了突破口。实际上,在他们之前,关于1918年大流感病毒的所有知识仅从18个档案标本中获得,Spencer等人发现的来自德国的3份含有病毒遗传物质的样本,为这场漫长的“破案”增添了一些新的线索。

“当我们拿到这些样本的时候,很明显,这对我们来说是一个重要的项目。”Spencer认为,这些新的线索和他们获得的结论仍然只是整个大流感故事中的冰山一角,“这项研究中3个完整的基因组、2个部分基因组和16个带有单一基因片段的样本,只能给我们一个非常粗略的概念。”他们的最新成果于近日发表于国际学术期刊《自然-通讯》(NatureCommunication),Spencer为通讯作者。
1918年和1919年发生了什么?大流感病毒最终又以何种方式“消失”于历史……探寻永远在路上。
永久冻土下埋藏的答案
眼下仍在全球高潮迭起的COVID-19大流体的病原体保持神秘的时间并不久。
疫情暴发初期,中国的研究团队在数天时间内从标本中检测出一种新型SARS样冠状病毒,并通过高通量测序获得了该病毒的全基因组序列。随后的2020年1月14日,世界卫生组织(WHO)正式将引发此轮肺炎的病毒命名为2019-nCoV(后被正式命名为“SARS-Cov-2”)。
值得一提的是,上述病毒全基因组序列的公布,是这场大流行中疫苗快速研发等相应抗疫举措的首要前提。
在一个世纪之前,这样的速度是不可想象的。尽管1918年有初步报告已经猜测,彼时的流感大流行是由病毒引起,但直到20世纪30年代这一猜测才被证实,当时有证据表明疾病与流感病毒有关。
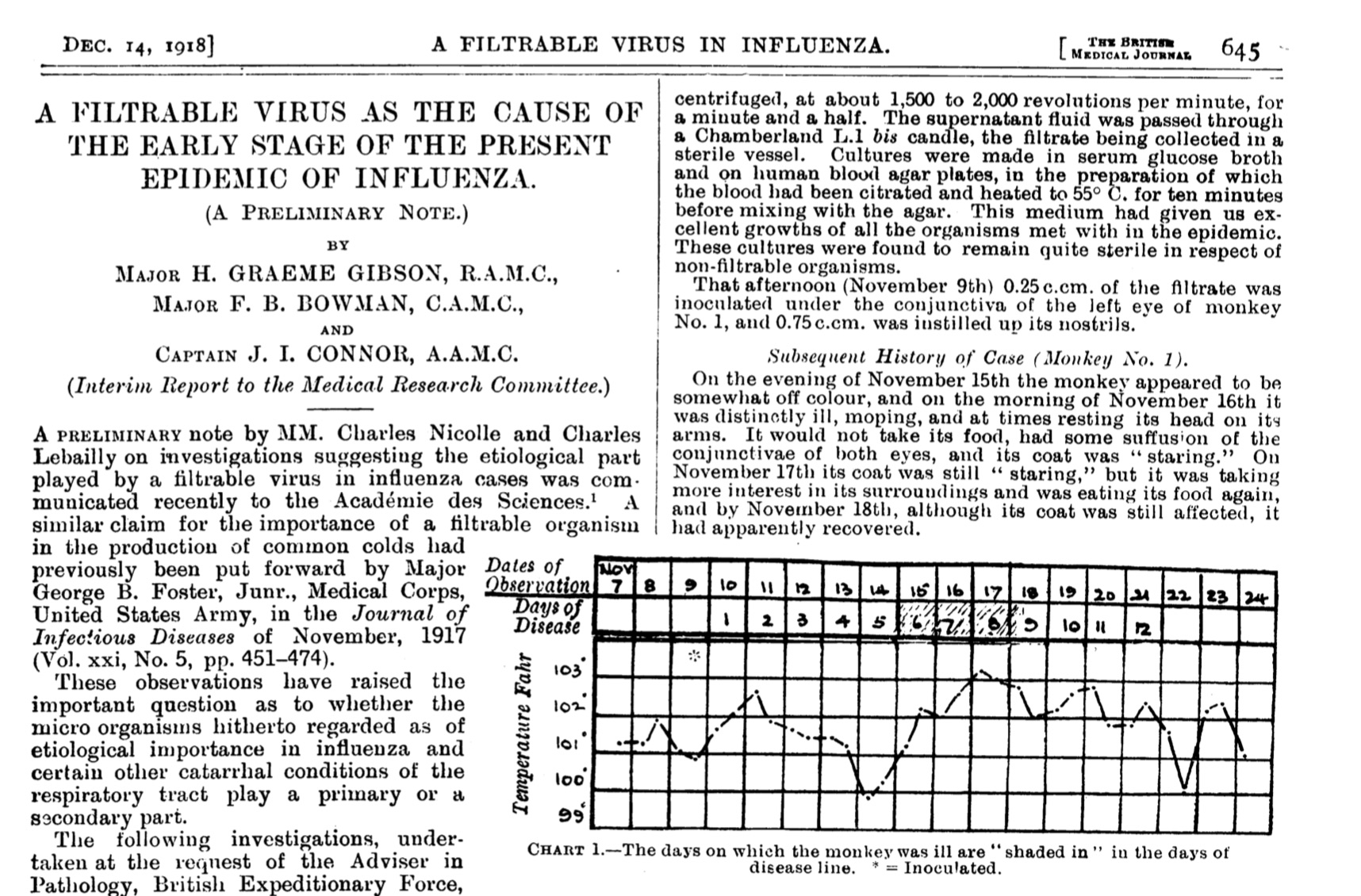
为了找寻早已“销声匿迹”的杀手,年轻的瑞典微生物学家、爱荷华大学博士生JohanHultin在1951年前往阿拉斯加州苏厄德半岛一个叫布瑞维格米申的海边村庄。那里的永久冻土之下,埋藏着科学界寻找已久的答案。
1918年11月,彼时的这一小村庄里约有80名成年人,大部分为因纽特人。但在当年的11月15日至20日的5天期间,流感大流行夺去了其中72人的生命。美国疾控中心官网对该事件的记录中写道,关于病毒是如何到达这个小村庄的,有不同的说法。然而,无论是附近城市的商人乘坐雪橇带来,还是当地的邮递员传播,它对当地人口的影响是有充分记录的。
村庄旁边的山上,当时的逝者被冻结在了永久冻土中,用小小的十字架标记。25岁的Hultin相信,在这片保存完好的墓地里,他或许仍能找到1918年病毒原本的痕迹。

阿拉斯加布瑞维格米申,1918年大流行时,这个小村庄的80名成年居民中有72人被埋在这里。
在当地允许之下,仅仅2天之后,Hultin发现了一具小女孩的尸体——保存完好,穿着一件蓝色的裙子,头发上装饰着红色的丝带。最终,Hultin成功地从埋在该地点的另外四具尸体上获得了肺组织。

1951年,Johan Hultin(左)和他的同事们第一次来到Brevig Mission。
然而,无论是物流难题,还是科学技术受限,从遥远的小村庄带回的样本并没有让Hultin找到他期望中的答案。
46年后的1997年,另一位年轻的分子病理学家、美国武装部队病理学研究所(AFIP)的JefferyTaubenberger等人在《科学》杂志上发表了一项研究,他们利用PCR技术,分别克隆了1918年大流感病毒的4条基因(HA、NA、NP和Matrix基因)的部分序列,并进行测序。通过有限的部分序列信息,Taubenberger基本确定了1918年大流感病毒是一种新的甲型H1N1流感病毒。

Taubenberger的团队从一名驻扎在南卡罗来纳州的21岁美国男性士兵的肺组织中提取了病毒的RNA。资料显示,1918年9月20日,这名士兵被诊断为流感感染和肺炎,住进医院。6天后,也就是1918年9月26日,他去世了,肺组织样本被收集并保存下来。
读到Taubenberger等人发表在《科学》上的这篇论文的时候,Hultin已经72岁了。他重燃了“侦探”到完整病毒的希望,并且写信给Taubenberger,询问对方是否有兴趣回到布瑞维格米申,从埋在阿拉斯加永久冻土中的1918年病毒受害者身上获取肺组织。
一周后,Hultin带着简陋的工具再次前往46前曾经去过的那个地方。流传下来的一个有趣细节是,他还借了妻子的花园剪刀来协助挖掘。Hultin自己支付了旅费,个人花费约32007美元,挖掘工作耗时约5天。但这次“远征”让他最终获得了非凡的发现。

72岁的Johan Hultin,时隔46年再次来到Brevig Mission。
在约7英尺深的永冻层中,埋葬着一名25岁左右(死亡时间)、肥胖的因纽特女人的尸体。她被Hultin命名为“Lucy”,脂肪保护了肺部组织免于腐烂,因此也保留了病毒的RNA。Hultin将肺组织取出,放入保存液中,然后分别运送给Taubenberger和他的同事们,包括武装部队病理学研究所的AnnReid博士。
10天后,Hultin接到了他期盼了半个世纪的讯息:科学家们确实从Lucy的肺组织中获得阳性的1918年病毒遗传物质。
随后的1997年至2005年,科学家们相继对1918年流感病毒的8条基因片段(HA,NA,NS1,Matrix,NP,聚合酶基因PA、PB1、PB2)的全基因组序列进行了测序。
尽管基因序列数据还是不能回答病毒的起源和流行病学特征,但这是几代科学家奋斗已久的里程碑成果。
“这类研究的最大困难显然是样本的稀缺性,而我们的分析必须要依赖这些微小的数据集。”Spencer对澎湃新闻记者如是表示。
首个来自欧洲的1918年大流感病毒基因组
在1918年流感病毒全基因组序列获得之际,Spencer正在法国里昂攻读博士学位,研究已灭绝棕熊(Ursusarctos)种群的遗传多样性和古病毒学。
2010年,Spencer来到了德国柏林,进入罗伯特·科赫研究所(RKI);2015年开始,他成为研究所的永久研究员,担任病毒进化组组长、高致病性微生物流行病学研究组副组长。目前其主要研究微生物多样性和进化(主要是病毒)、撒哈拉以南非洲的人畜共患病和哺乳动物的多样性。
Spencer提到,当他们开始这项工作之前,关于1918年大流感病毒的所有知识仅从18个标本中获得,并且没有关于大流行早期阶段的全基因组信息。
总体而言,1918-1919年大流行期间,第一波春季潮开始于1918年3月,并在接下来的6个月不同程度的扩散至美国、欧洲甚至亚洲,患病率非常高,但多数地区的致死率并没有显著高于正常值。第二波秋季潮开始于1918年9-11月,迅速在全球蔓延且高度致命。第三波流行潮则始于1919年初。
他们在论文中详细提到,从20世纪90年代末确定了病原体为甲型 H1N1流感病毒起,科学家们从1918年9月死于纽约阿普顿营(简称CU)和1918年11月死于阿拉斯加布瑞维格米申(简称BM)的病例身上,重建了两个完整的基因组。此外,科学家还从1918年5月至1919年2月期间死于流感的美国(n=14)和英国(n=2)的其他流感死亡者身上获得了15个血凝素(HA)基因的部分序列和1个完整序列。
Spencer等人认为,这些序列为了解1918年大流行的起源、后果以及病毒表型提供了一些见解。1918年大流感病毒所携带的至少7个片段(HA除外)似乎来自于禽宿主中传播的甲型流感病毒(IAV株)的多样性,这些片段被传播给季节性H1N1流感病毒。此前也有研究显示,对基于上述BM病例基因组序列的传染性1918大流行病毒重建表明,血凝素和聚合酶复合基因可能是该病毒致病性的主要决定因素。
然而,由于信息的缺乏,许多问题仍未解决或仍在争论中。Spencer等人提到,例如,在大流行期间产生了多少基因组多样性?在大流行高峰前和高峰期间观察到的严重程度的变化是否归因于不同的病毒遗传特征?在随后的季节性H1N1病毒中,血凝素的起源是什么?
“任何新的基因组,都可以增加我们的知识。”但Spencer同时补充道,这些大多保存在福尔马林中的标本在过去和现在都有着不好的“名声”,“难以合作。”
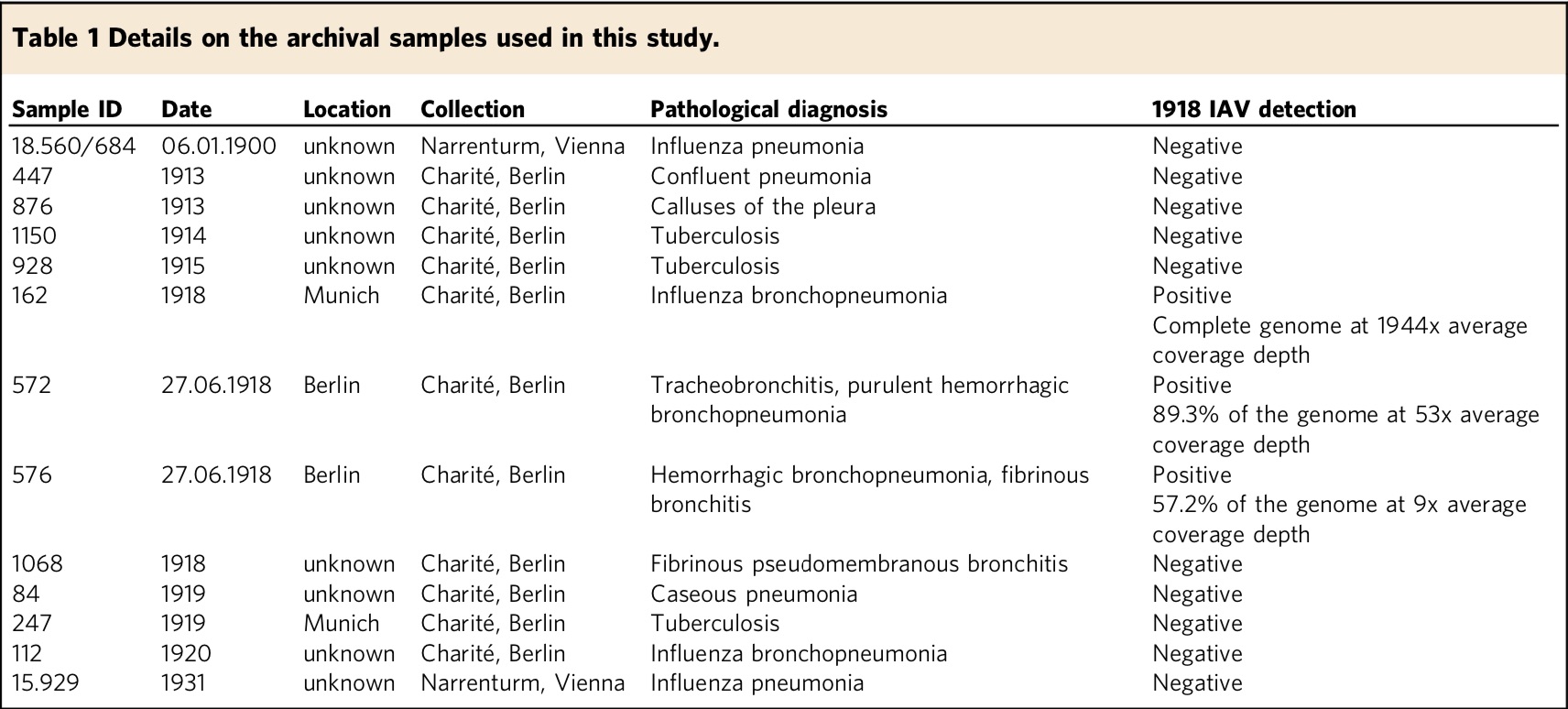
为了探索大流行不同阶段病毒之间的差异,研究团队选择了1900年至1931年之间的13份由福尔马林固定的肺部标本,这些标本保存在柏林Charité(n=11)的和维也纳Narrenturm(n=2)的病理博物馆中。这组标本包括了欧洲大流行期间收集的6个标本(1918年4份, 1919年2份)。
这些组织此前经福尔马林固定石蜡包埋的方法(FFPE)处理,想要提取出其中的核酸并非易事。研究团队将豌豆大小的肺片洗净处理,热处理逆转福尔马林造成的大分子交联,进行核酸提取。之后的步骤就是建立高通量测序文库,然后进行测序。
“我认为这篇论文最酷的部分是,他们能够从这些福尔马林固定的组织中提取出这些序列。”没有参与这项研究的佛蒙特大学拉纳医学院的病毒学家EmilyBruce评价道。
Spencer也谈到,永久冻土层保存的尸体和大流行死亡者的病理标本非常罕见,获取大量基因组可能是无法做到的。而从档案样本中提取核酸的最新进展,让他们有了对这些探索研究过的欧洲病理学样本探索的机会。
研究团队获得3份1918年大流感病毒的阳性样本,即MU-162(慕尼黑)、BE-572(柏林)和BE-576(柏林)。
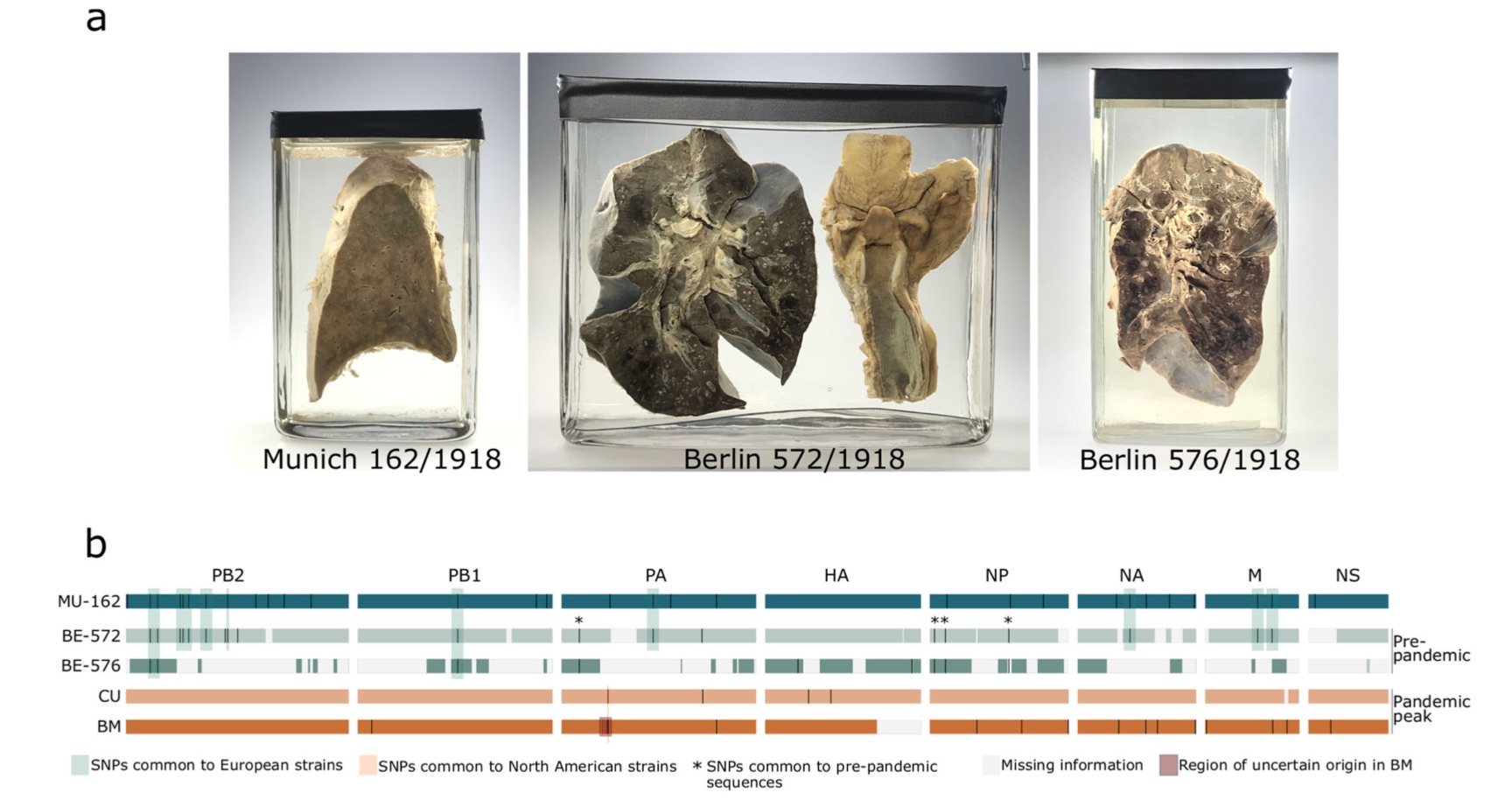
论文细节显示,MU-162取自1918年死于慕尼黑流感相关肺炎的一名17岁女童,具体采集日期没有报告。病理表现为化脓性支气管炎、细支气管炎和双侧合并支气管肺炎;BE-572样本取自1918年6月27日死于柏林的一名18岁男性士兵。病理表现为严重脓性假膜性气管支气管炎和脓性出血性支气管肺炎;BE-576样本取自1918年6月27日在柏林死于流感的另一名17岁男性士兵。病理表现为纤维性支气管炎和脓性出血性支气管肺炎。
研究团队对这些样本进行测序,分别获得40.133.161、31.989.479和14.965.377的高质量读长。这允许他们重建MU-162的完整的1918流感病毒(平均覆盖深度为1944x),以及BE-572和BE-576的部分基因组(分别为89.3%和57.2%,平均覆盖深度分别为53x和9x)。
这里需要指出的是,上世纪70年代兴起的DNA重组技术,是生物医学领域具有里程碑意义的事件,这使得人类可以对DNA进行克隆和改造。美国纽约西奈山医学院著名的微生物学家PeterPalese博士和AdolfoGarcia-Sastre博士在1999年就开发了将流感病毒基因组克隆到特殊的DNA载体,产生重组活流感病毒的技术(反向遗传学技术),这项技术是研究流感病毒基因功能有效的遗传学工具。
这项技术为重建1918年大流感病毒铺平了道路。然而,对于重建20世纪最致命的流感病毒的决定,仍然是在相当谨慎的情况下做出的。这项重建工作最后由受过训练的微生物学家TerrenceTumpey博士一个人完成,地点被指定在亚特兰大的美国疾控中心总部。

Terrence Tumpey博士。
Tumpey的工作始于2005年夏天。为了减少对同事和公众的风险,他被要求独自研究这种病毒,而且只有在同事们下班回家的几个小时之后。进入BSL-3E实验室需要进行生物指纹扫描,而病毒冷藏库只有通过对他的眼睛进行虹膜扫描才能进入。Tumpey还被要求每天服用规定的预防剂量的流感抗病毒药物奥司他韦,防止受到感染。
当1918年大流感病毒在他的细胞培养中出现的那一天,Tumpey在一封邮件中写道,“这是我的一小步,是人类的一大步。”
Spencer表示,重建MU-162的完整基因组,这是北美以外、首个来自欧洲的1918年大流感病毒的基因组。另外至关重要的一点是,他们也获得了第二波秋季高峰期前的样本。
样本的获得弥足珍贵,Spencer同时谈道,“我们不知道这个样本的代表性如何,但显然,如果考虑一个维度,比如地理因素,我们有了一个数据集。”他希望,来自欧洲样本的研究能为将来的进一步努力打下坚实的基础。
古老的肺部“遗书”:读到了哪些信息?
结合上述提到的此前已有的BM和CU序列,研究团队首先利用这些新获得的德国流感病毒基因组评估了不同地理位置和不同月份的毒株的基因组多样性。
分析显示,1918年6月从柏林采样的两个部分基因组在HA基因片段中最多两个位点存在差异,这表明在当地和当时的时间点,疫情内的可变性可能可以忽略不计。当将几乎完整的来自柏林的BE-572基因组与来自慕尼黑的另一个德国序列(MU-162)进行比较时,发现了22个SNP(单核苷酸多态性),与此前报道的两个北美基因组的差异相似。欧洲和北美基因组的比较显示出22-43个SNP。
研究团队还将大流行高峰期前的欧洲BE-572基因组((1918年6月)与大流行高峰期基因组CU(1918年9月)和BM(1918年11月)进行比较,分别鉴定出22和29个SNP。
他们认为,总的来说,这些比较表明,存在可测量的基因组可变性,在相同大陆(0.11-0.16%)和在大流行同期(0.11%)采样的基因组比在不同大陆(0.16-0.32%)和不同时期(0.16-0.21%)采样的基因组总体差异更低。
这就意味着,这些基因组多样性与本土传播和长距离扩散相结合的事件也是一致的。
为了评估观察到的基因组差异是否有表型影响,研究团队进行了体外探索性研究。他们发现,BM的聚合酶活性比MU-162高2倍。为了确定导致这种差异的亚基,他们通过在BM和MU-162之间交换单个聚合酶亚基来进一步分析。将PA从MU-162引入到BM聚合酶复合物中,其活性降低了1.7倍。与这一发现一致,BMPA使MU-162聚合酶的活性提高了1.7倍。PB1和PB2亚基的交换对活性也有类似的影响,但影响较小。NP交换则无影响。

为了更精确地确定所观察到的表型差异的遗传决定因素,研究团队还生成了BM点突变体,每个突变体携带MU-162病毒中发现的一个氨基酸(aa)变化。最后发现分布在PA(3)、PB1(1)和PB2(1)的5个突变显著降低了聚合酶的活性。
这些结果表明,在体外,这些氨基酸变化影响了病毒RNA聚合酶复合物的活性,而聚合酶复合物在平衡病毒毒力中起关键作用。
他们同时强调,观察到的差异是否会转化为独特的表型仍然存在很多不确定性。但他们的结论是,如果这项研究的发现不一定能够预测体内功能差异,那么在现阶段,这符合1918年流感病毒表型多态的概念,应该鼓励未来对这个问题的研究,使用更多的病毒序列和可能的重建病毒。
研究还进一步分析了1918年大流感流行期间病毒的地理传播和功能演变。Spencer等人认为,研究支持了大流行病毒跨大西洋移动的假设,与第一次世界大战末期人类迁徙的历史背景一致。

美国疾控中心对1918年大流感的历史介绍中也同样提到:1918年,一种新的流感病毒出现了。与此同时,第一次世界大战正在进行。第一次世界大战的条件(过度拥挤和全球军队调动)促进了1918年流感的传播。
研究团队认为,总之,基因组数据支持了一种以本地传播为主、伴有频繁的远距离传播事件的情景。
他们还使用了相同的HA序列数据集,关注了不同时期病毒之间的进化关系。他们的数据强烈支持与单一的单系谱系不同的另一种情况,即多个大流行高峰前谱系在接下来的大流行几个月都存活了下来。
针对第一波和第二波大流行之间致病性的差异,Spencer等人还专门研究了病毒可能在大流行高峰期前和高峰期之间出现的适应性,并可能导致后者的严重程度增加。aa残基G222存在于H1亚型HA蛋白受体结合域,该残基对禽类和人类聚糖都具有结合亲和力,而类人D222只有效地结合人类聚糖。
这项研究中最新测序的3株德国HA已携带了类人D222,研究团队认为,这降低了这两种变异在大流感流行高峰前和高峰期间发生显著变化的可能性。
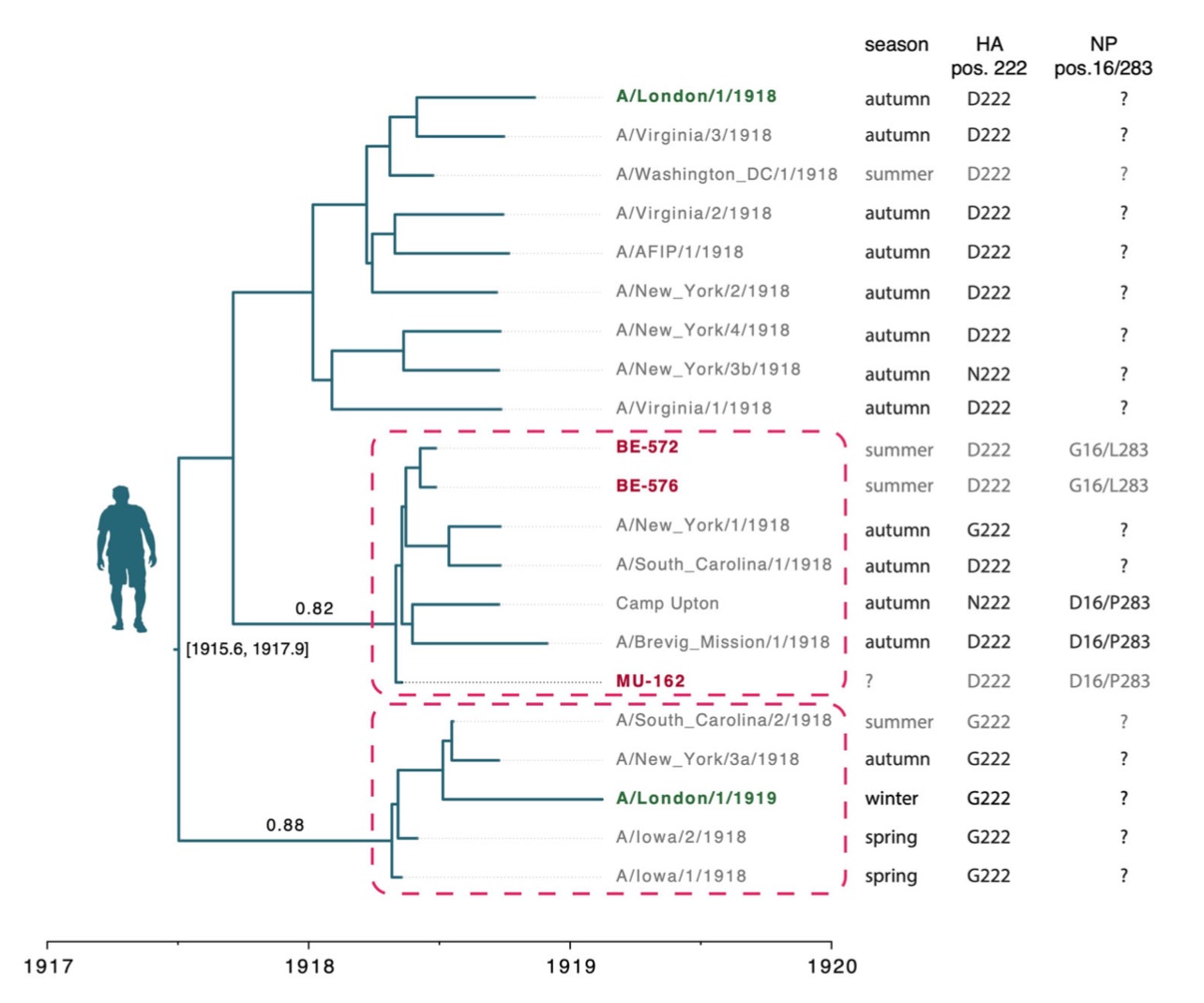
但他们同时识别出另外两种可能标志着流感高峰期和流感高峰期之间重要区别的aa变化。他们发现,高峰前毒株BE-572和BE-576携带NP位点16(G)和283(L)禽类残基,而高峰期毒株和MU-162(采样日期未知)携带D16和P283。这两个位点已知会影响干扰素诱导的MxA抗病毒蛋白的宿主范围和易感性/耐药性。
研究团队认为,这些突变可能代表了早期适应人类的特征:在其传播的最初几个月,1918年流感病毒可能进化出更好的躲避先天干扰素反应的能力,这是流感病毒致病性的一个重要方面。
值得关注的是,研究团队通过分析还认为,在1918年流感大流行结束后开始传播的季节性H1N1流感病毒(直到1957年H2N2流感大流行被取代),是流感大流行病毒的直接后代。值得注意的是,随后的1968年,H3N2流感病毒取代H2N2病毒,引发大流行;2009年,H1N1流感病毒再现。
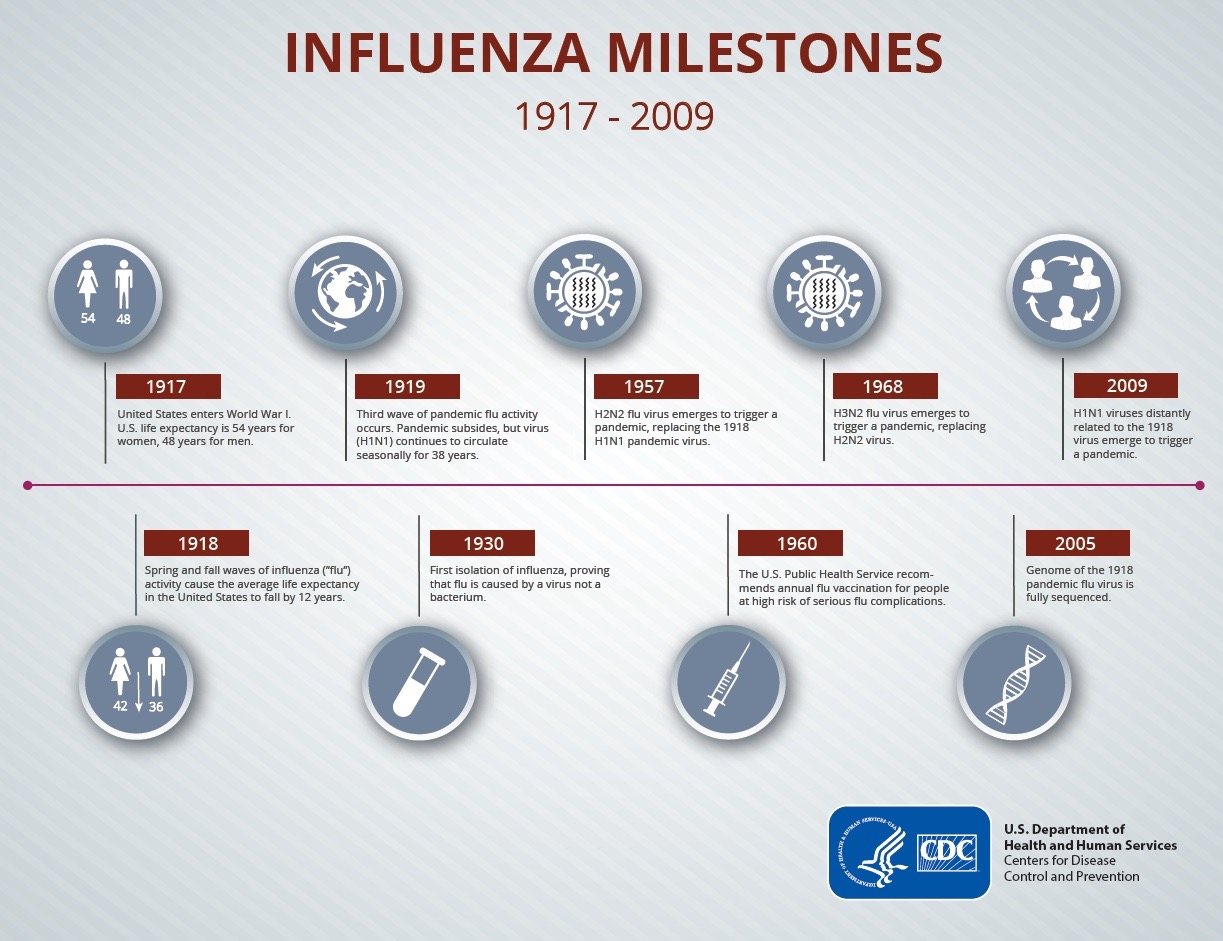
科学家们此前就曾将1918年大流感与随后的季节性流感联系起来。在过去,有研究提出,大流行后出现的季节性H1N1病毒是重组的结果,即感染同一宿主细胞的病毒之间基因交换,这意味着与其他流感病毒交换基因后病毒可能变得不那么致命。
Spencer等人在这篇论文中写道,新的分析符合季节性H1N1病毒可能是由大流行流感直接演变而来,不需要重组。然而,研究同时强调,鉴于建模方法的局限,目前证据还不能让他们完全肯定地支持该结论。
Spencer对澎湃新闻记者总结称,他认为,相对频繁的跨大西洋传播是可信的。另外,1918年流感大流行的第一年,多种流感谱系持续存在。而第一波和第二波大流行比较的两个基因组中存在潜在的适应性。
他同时强调,为了更好地了解这场大流行,需要获得更多的基因组。以他们在这项研究中的最后一个结论,即季节性H1N1病毒可能是由大流行流感直接演变这一点来说,“可以通过在大流行期间和20世纪20年代进行更多采样来加强研究。”可惜的是,“后面这10年没有进一步数据。”Spencer表示。
Spencer最后谈到,其研究过去流行病的动机之一,在于“希望找出共通的一些规律和模式。”放置在当下COVID-19大流行之下,他尤其提醒,“了解共同特征和差异将有助于我们做好准备。”
